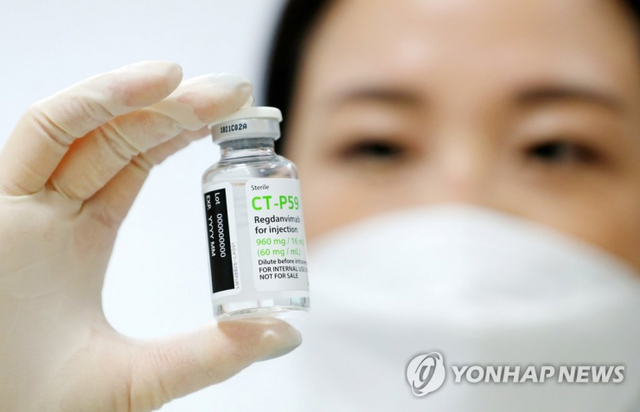
[천지일보=홍보영 기자] ㈜셀트리온의 신종 코로나바이러스 감염증(코로나19) 항체치료제 ‘렉키로나주960mg(레그단비맙)’가 임상 3상 시험을 전제로 두 번째 전문가 자문 심의에서 허가 권고를 받았다.
27일 식품의약품안전처(식약처)는 ‘렉키로나주’의 안전성과 효과 등에 대해 자문하고자 회의를 연 결과 ‘중앙약사심의위원회(중앙약심)’이 3상 임상시험 결과를 제출하는 것을 조건으로 품목허가를 권고했다고 밝혔다.
다만 중앙약심은 “경증 환자에 대한 이 약 투여의 임상적 의미는 결론을 내리기 어렵다”며 중등증 환자와 고위험군 경증 환자를 대상으로 이 약을 투여할 것을 권고했다.
구체적으로 중앙약심은 ▲실내 공기에서 산소포화도가 94%를 초과하는 자 ▲보조적인 산소 공급이 필요하지 않는 자 ▲투여 전 7일 이내에 증상이 발현한 자 등 세가지 조건을 모두 충족한 환자에게 이 약을 사용할 것을 권고했다.
오일환 중앙약심 위원장은 “이 약 투여 후 안전성과 관련해 업체가 제출한 자료를 바탕으로 현재 수준에서 생명을 위협하는 중대한 이상사례는 발생하지 않았다”면서도 “충분한 환자 수를 대상으로 3상 임상시험과 시판 후 지속적인 안전성 평가가 필요하다”고 권고했다.
그러면서 “다만 일부 위원들의 경우 소수의견으로 의약품 품목허가보다는 특례 제조 승인 등을 활용하는 것을 제안했다”고 밝혔다.
식약처는 “셀트리온 렉키로나주와 관련한 품질자료 일부 등 심사자료를 제출받아 검토를 진행하겠다”며 “‘코로나19 치료제 안전성·효과성 검증 자문단’과 이번 중앙약심 자문을 통해 얻은 전문가 의견, 효능·효과(안), 권고사항 등을 종합해 ‘최종점검위원회’를 통해 렉키로나주의 허가 여부를 최종결정할 예정”이라고 덧붙였다.

